一文读懂最新AI医疗器械产品审批要点
6月28日,国家药品监督管理局医疗器械技术审评中心官网公布了深度学习辅助决策医疗器械软件审评要点及相关说明。审评要点包括五个方面:适用范围、审评关注重点、软件更新、相关技术考量、以及注册申报资料说明。
1.适用范围
适用范围包含以下三种情况:
深度学习辅助决策医疗器械软件(包含独立软件、软件组件);
使用深度学习技术进行前处理、流程优化、常规后处理等非辅助决策的软件;
使用传统机器学习技术的软件。
遵循的原则包括:
《医疗器械软件注册技术审查指导原则》
《医疗器械网络安全注册技术审查指导原则》
《移动医疗器械注册技术审查指导原则》
不含人工智能伦理、数据产权等法律法规层面要求
2.审评关注的重点
审评关注的重点在于软件的数据质量控制、算法泛化能力、临床使用风险,临床使用风险应当考虑数据质量控制、算法泛化能力的直接影响,以及算力所用计算资源(即运行环境)失效的间接影响。
此类软件监管基本方法是基于风险的全生命周期管理,主要有以下几方面的考量:
1.软件风险管理。其中软件临床使用风险主要包括假阴性(漏诊)和假阳性(误诊)。
2.软件设计开发:包括四个过程
需求分析 数据收集 算法设计 验证与确认
需求分析重点考虑数据收集、算法性能、临床使用限制等方面要求。
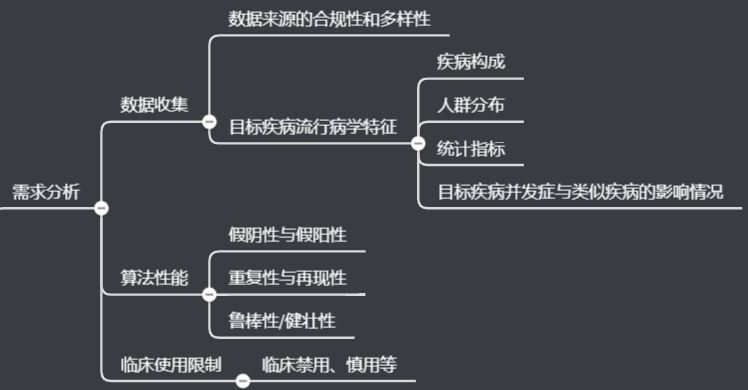
数据收集又包括数据采集、数据预处理、数据标注、数据集构建四个部分。

数据采集
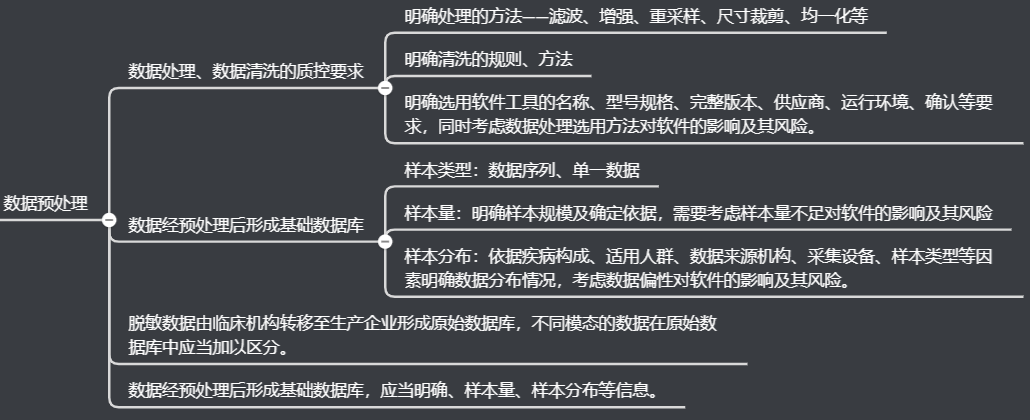
数据预处理

数据标注

数据集构建
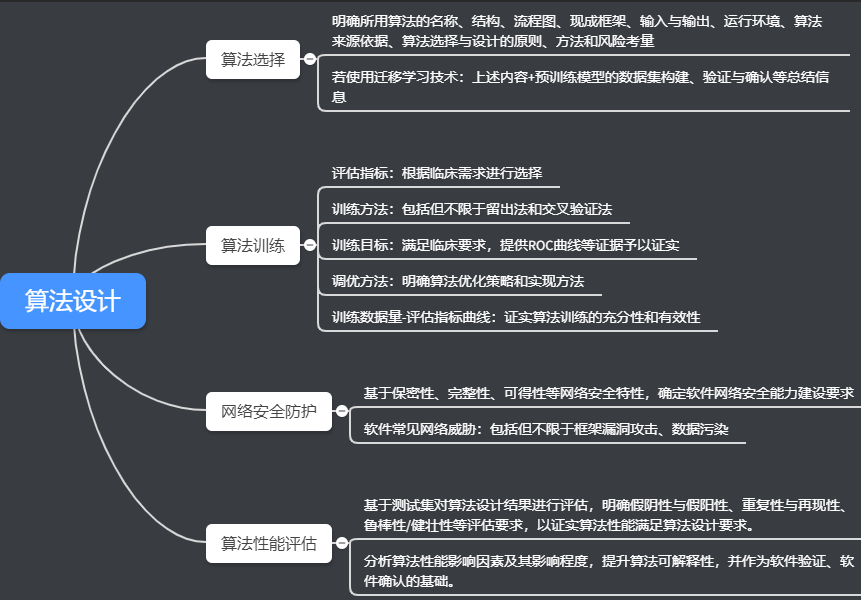
第三个部分算法设计从算法的选择、训练、网络安全防护以及算法性能评估等方面做出规定。
第四部分,验证与确认,包括软件验证和软件确认两部分。
软件验证包括软件验证测试、设计评审等。
软件确认则要通过临床评价的方式进行,遵循《医疗器械临床评价技术指导原则》、《医疗器械临床试验质量管理规范》、《医疗器械临床试验设计指导原则》等要求,基于软件的预期用途、使用场景和核心功能进行试验设计,确认软件的安全性和有效性。
进口软件应当提供中外人种、流行病学特征、临床诊疗规范等方面差异影响的临床评价资料,若不足以证实申报产品在中国使用的安全性和有效性,应当在中国开展临床试验。使用境外临床试验数据应当满足《接受医疗器械境外临床试验数据技术指导原则》要求。
此外,临床评价可采用基于现有历史数据的回顾性研究,基于软件安全性级别考虑使用问题。此处对于安全性级别进行了划分,包括A、B、C三类。
安全性级别为A、B级的中低风险软件回顾性研究可用作临床预实验或替代临床试验。
安全性级别为C级的高风险软件,回顾性研究可用作临床预试验,为临床试验设计提供参考依据,或者在少见亚组病例入组时间过长等情况下,用作临床试验的补充。
3.软件更新
软件更新分两类,重大软件更新和轻微软件更新。
重大软件更新包括软件更新的基本类型,以及算法驱动型和数据驱动型,此类更新应当申请许可事项变更。
其中算法驱动型和数据驱动型软件更新应当开展算法性能评估、临床评价等验证与确认活动,临床评价应当与软件安全性级别相适宜。
轻微软件更新无需申请许可事项变更,通过质量管理体系进行控制。
软件版本命名要涵盖算法驱动型软件更新和数据驱动型软件更新,明确并区分重大软件更新和轻微软件更新。其中重大软件更新应当列举全部典型情况。
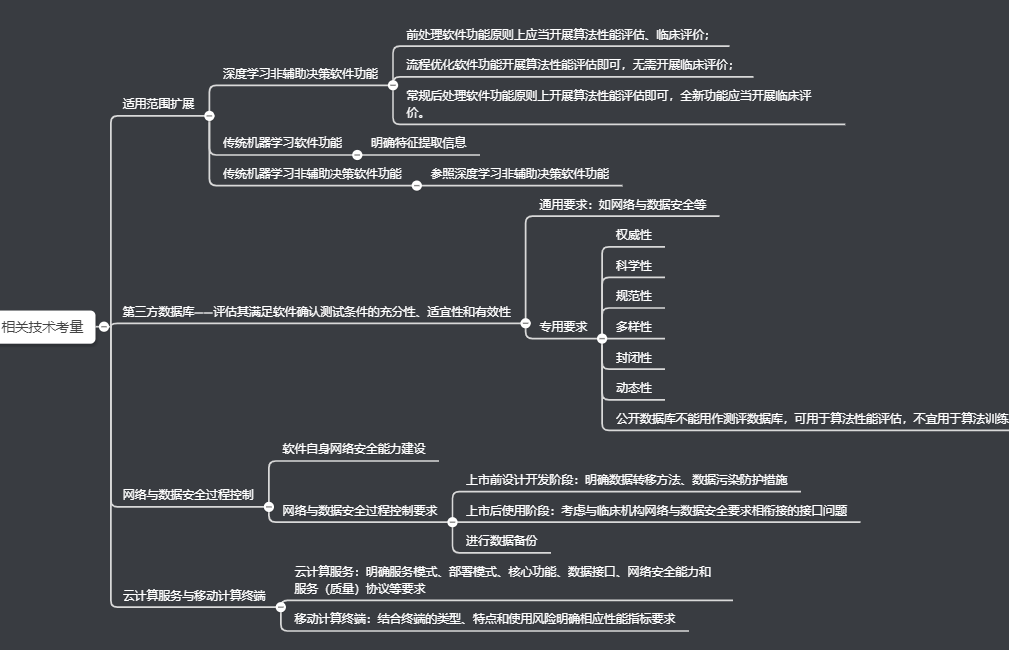
4.相关技术考量
相关技术考量包括适用范围扩展、第三方数据库、网络与数据安全过程控制、云计算服务与移动计算终端四个方面。
5.注册申报资料说明
前提是要满足软件指导原则、网络安全指导原则、移动器械指导原则等相关指导原则要求。此外,还包括以下要求:
第一,产品名称应当符合独立软件通用名称命名规范要求,体现处理对象、目标疾病、临床用途等特征词。
第二,对于适用范围的要求:辅助决策独立软件应当明确预期用途、使用场景和核心功能;软件组件参照辅助决策独立软件要求。
第三,研究资料
1)软件描述文档、网络安全描述文档、软件版本命名规则。
2)软件描述文档核心算法部分应当结合本审评要点提供相应算法研究资料。
3)研究资料“其他资料”应当提供网络与数据安全过程控制研究资料(“其他资料”包括公开数据库、测评数据库的基本信息和使用情况)。
第四,说明书
首先应当符合《医疗器械说明书和标签管理规定》要求。
说明书内容包括:
辅助决策软件说明书:
明确软件的适用范围、临床使用限制、注意事项、用户培训、采集设备要求、数据采集操作规范、输入与输出、算法性能评估总结(测试集基本信息、评估指标与结果)、软件临床评价总结(临床数据基本信息、评价指标与结果)、运行环境等内容。
深度学习辅助决策软件说明书:
除上述内容外还应当补充算法训练总结信息
基于以上信息,医疗器械软件注册申报的条件和流程已经有了详细规定,AI医疗器械厂商的产品研发落地申报有了新的指引。

关注大健康Pai 官方微信:djkpai我们将定期推送医健科技产业最新资讯



